第二轮的4+7,已经在路上了
2018年“4+7”政策的影响无疑是巨大的,有的新产品刚拿到批文,可能就没法做了……
但无论你怎么看,无论你高兴与否。据说,第二轮的“4+7”已经在路上了。
本文将把招投标放在一个竞争的角度,尝试分析影响结果的各种力量,以及彼此之间的关联。
大致分为以下几个章节。所有力量将在各自章节粉墨登场,展现自己的实力。
-
环境分析(国际,国内)
-
“4+7”的影响
-
企业和个人的选择
环境分析:国际,国内
中国加入ICH,药物质量标准与国际接轨

ICH是发达国家的最低标准,中国过去药物政策法规很大程度上是遵照WHO(世界卫生组织)的标准(较低)。
*ICH,即人用药品注册技术要求国际协调会(International Council for Harmonisation of Technical Requirementsfor Pharmaceuticals for Human Use) 。是由美国、日本和欧盟三方的政府药品注册部门和制药行业在1990年发起的,主要目的是协调全球药品监管系统标准化。
2017年,中国正式成为ICH成员,承诺全面提高药品生产企业的监管标准。对于监管部门而言,一致性评价是和国际接轨的条件之一,是准入“标准”问题,而非企业认为的“提价”条件。
国内监管从严,控费从紧
在这里主要想理解政府的目的,以及招标决策的主体的彼此关系以及如何互动。
①政府的目的是医改
“医改”包含了药品市场的“增量”和“存量”改革以及“分级诊疗”推进,并互为因果,互相制约。
“增量”主要体现在“创新药审评审评”“医保准入”的提速。但是,由于审批资源有限,在阶段性目标实现后,提速可能后会放缓。
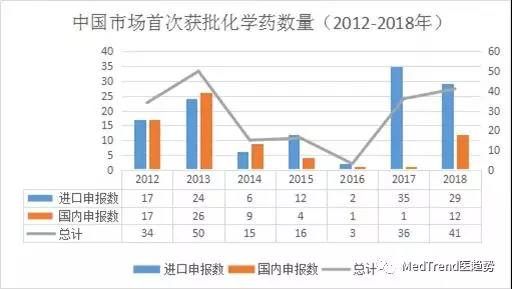
▲中国市场首次获批化学药数量2012-2018年(图自医药经理人)
“存量”治理,手段之一就是招标。官方说法是,医保局是招采的职能部门。但实际上,医保局招采司在4+7地区主导采购。4+7以外地区,医疗机构和卫健委均能干预采购。所以我们要从医保局和卫健委以及医疗机构一起看。
②决策的主体彼此如何互动
首先,无论谁招采,最后都面对支付问题。钱谁出?答案是医保局。所以“钱袋子”要主导招采。
筹钱主要来自以下几方面;
-
工资单,可以比较一下自己的“医疗保险”扣除金额,羊毛出在羊身上

▲来源个人工资明细
-
居民医保,新农合,属于定额投入,增长有限(30元/年左右)
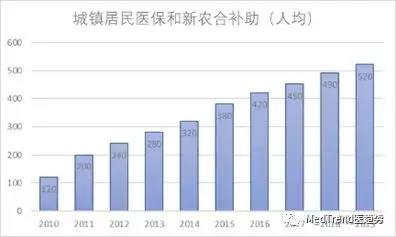
▲城镇居民医保和新农合补助(人均)
医保的筹资途径是有限的,且每年相对金额固定。
看完筹资,再看花钱;
2016人口抽样调查45-75岁人口占总人口35%;
2017年的医院出院统计,45-60岁占出院人数60%。
其中,肿瘤占76.7%,循环系统疾病占了91%。
那么慢性病和大病(肿瘤)药物就会成为医保支出的大户,且随着老龄化基数逐渐增加。而且,将来医保支付面会进一步扩大,新增花钱的地方。
2019年3月5日李克强总理《政府工作报告》指出:
“统一降低大病保险的起付线”。
“高血压,糖尿病等门诊用药纳入医保报销”。
这就像以前生了很多孩子的家庭,想吃饱怎么办?那就买菜的时候狠狠的杀价吧。
其次,看卫健委。
卫健委主任,马晓伟在3月8日的谈2019年在分级诊疗制度方面解决四大问题:
第一,以学科建设为抓手,做到区域分开,缓解北上广的医疗压力;
第二,就是以县医院为抓手,解决城乡分开;
第三,以病种为抓手,解决上下分开(常见病、多发病在社区、在基层,疑难重症在大医院);
*2018年,国家卫健委印发《疑难病症诊治能力提升工程项目储备库的通知》。将113所医院纳入工程项目储备库,可能会逐步关掉普通门诊。把常见病,通过医联体的延展服务留在下级医院。
第四,以支付方式改革为抓手,解决急慢分开(要用医保价格调节杠杆发挥作用,把慢性病的住院资源给到急症住院患者)。
前三条翻译过来是,
-
与慢病相关的仿制药市场向基层转移;
-
受影响最大的是重点病种,高血压、糖尿病、肿瘤、心血管疾病……
第四条,看到没“医保价格调节杠杆发挥作用”,也就是绕了一圈还是回到医保局付费。
-
实际上,县级医院面临医保资金的风险。例如农民看病,门诊花费上千元,如果不住院农民就报销不了,但安排不必要的住院势又浪费医疗资源;
-
慢性病药多了,药占比考核也会上升。
所以,反观各地,虽对外是”价格不公开“但实际却是“默许”价格联动。
一致性评价的标准加上各地的价格联动,织就一张网,不受波及的地方是很少的,这也是4+7影响大的原因。
比如:除4+7城市的已中标品种降价外,未中标价目前已经有上海、北京、辽宁、天津启动梯度降价。最新消息,北京说“未中选的一致性评价品种,取上海谈判价和全国最低价中的低价,作为北京谈判参考价”自己体会体会。
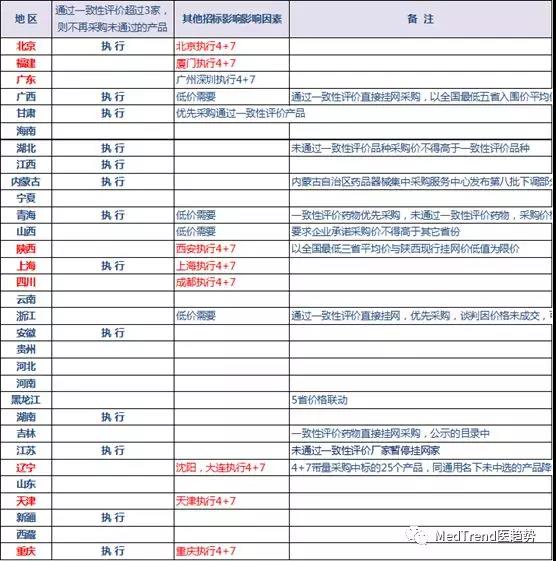
▲各地一致性评价的影响情况
让我们来到出发的地方,会发现11个城市试点,其实不仅仅只是测试,而是一开始就冲着实际问题去的。
为什么这么说?
用2017年的医疗卫生机构收入与支出做计算后,发现:4+7所在的省份卫生收入占全国的37%,但卫生支出占比高达50%!
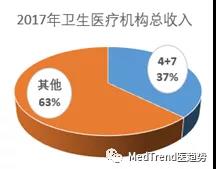

4+7虽说是11个城市,但这些城市在其所在地区的示范作用,导致直接和间接影响的范围其实很大。
以省为单位进行计算如下:
诊疗人次数占全国的44%,门急诊占全国的30%。容易发挥头部效应。
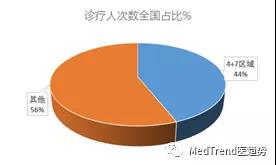
测试结果如何呢……
“4+7”有什么影响?
-
一石多鸟,“市场反馈超预期;
第一轮“4+7”后,可以肯定的是,阶段性目标达成远超预期
-
政治层面,老百姓喜闻乐见;
-
中标产品的价格制约了其他药物维持高价;
-
某一类疾病总的治疗成本相对固定,“临床路径”和“药占比“的“控费”目标得以实现;
-
“原研药贵有贵的道理”失去意义,外企会主动降价 ;
(第一轮4+7后,为缩短决策流程,辉瑞已经将仿制药总部移到中国)
-
第一轮的结果,可能结果强化了决策层对“药价虚高”的固有观点。
(3月11日,北京阳光采购通告,体现了决策层对当下的认识,取最低参考价)
目前,有184个品规通过了一致性评价,第一轮4+7进行了31个产品采购,成交25个,还余80多个品规,约20个左右产品,为第二次招标提供了标。
据说占市场80%的药品约200个左右,那么每次“4+7”约20-30个药品,所以第一轮后,也需要继续1-2轮覆盖剩余的产品。
虽然,第一轮招标后,市场也传来不同的声音,但可能不足以影响决策者改变。
-
单一最低价中标模式需要改进;
防止低价倾销,多家中标代替独家中标等。但实际监管加强后,质量是硬指标。其次,独家也只享有70%市场并非100%,且上海通过提高的自付比例,把决定权给了患者自己。
-
仿制药质量提升需要政策鼓励;
大概是因为“优质才能优价”的预期利空。个人认为持这种想法更多出于企业自身考虑,而缺少对国际和国内的竞争角度的分析。
-
一致性评价标准问题;
目前CDE要求体外药学一致,体内生物等效性(BE)也要通过,并且要求空腹和餐后均须完成。而国外大多数药监机构均只要求空腹BE即可。且BE一项费用在400-1500万,成为企业难以承受之重。但如果同一赛道里有多家企业竞争,这就成为典型的“囚徒困境”,无解。
-
注射剂、中药、中药注射剂及其他剂型的再评价政策仍不明朗。
综上,启动时,外界理解为市场机制实现控费;但实际发生说明行政干预是强势存在。新政策密集出台,波及效果如同多米诺骨牌。
企业和个人的选择
选项很少。目前,中国有7000多家药品生产企业,其中4300多家是制剂企业。据说卫健委计划将医院用药将集中在1200个范围,约占整体药品的70%左右。
那么网传的日后千家药企规模(其中500家左右仿制制药生产企业和部分创新药企业),应可以满足上述市场需求。
应对方向大概归结3类。
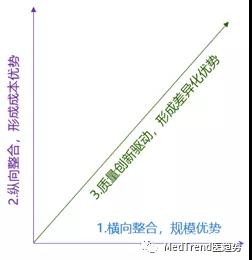
(图自毕马威报告)
①横向协同,强化在某一领域和科室的的集团作战优势
由于竞争环境复杂,单纯的执行能力将不再适合市场需要;而能在复杂医疗场景识别商业机会,并整合市场,销售,医学等多方资源实现项目营销的人会成为必然选择。
能力模型:销售+市场+医学;也许很难全部打通,但个人发展必然受限于技能单一。
②产业链竞争,将产业链上各环优势层层累加,形成整体优势
比如整合了原料药的企业,可以在价格上形成优势,进行“薄利多销”的规模化营销。临床费用取消,销售团队缩减或取消。
③研发技术壁垒,放大一致性评价的产品数量,抢占一致性评价前三的位置
招标的准入条件对研发,医学,市场准入部门均提出了很高的要求,分水岭是专业能力的前瞻性。
为适应商业模式的创新,个人除了需要横向协同能力,还需具备对行业有“点线面”深刻认知,并从中搭建“赋能”的平台。
作为个人,外界变化属于不可抗力,但至少可以为模式1和3做准备,从而顺应趋势。
总结
4+7及其他招标变化,是政府机构改革的外在表现,控费是目标。
医保招采司和卫健委和医疗机构联动,行政干预加强,买方处于强势地位。
公立医院市场,一致性评价是硬指标,特例除外。
第一轮4+7提示,仅从企业的角度分析政策会误判,仿制药向“规模化”营销转变是大概率。
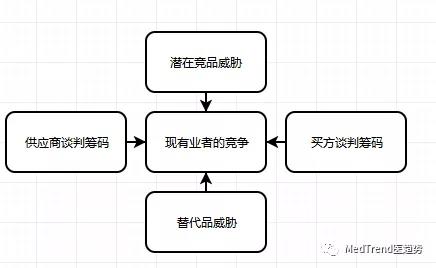
▲医药企业间的竞争
加入ICH后,国际仿制药进入会加快。换言之,不能只看国内竞争者。
药品之后就是器械和耗材了。
政策解读,以及商业模式转变,体现在更多维度。所以个人的单一技能不足以获得长期竞争优势。
CRO公司红利增加,CSO可能萎缩,培训产业受冲击。
面对未来的挑战,我觉得应该向华为学习。任总面对美国的封锁时说:
“我们从来没有认为美国对我们不好,美国从一个弱国变成大国,因为开放。华为要跟他们学习开放。华为在世界上的地位不是要把谁当竞争对手,未来社会是个很复杂的社会,我们要去确定未来的思想理论结构是什么,我们没有把任何人当敌人,要共同创造世界。”
从话里我提炼了三点:要开放(对治僵化),底层逻辑和方法论是根本(对治侥幸和速胜),互相赋能才能共赢(驱动市场的力量是多维的)。
信息来源:MedTrend医趋势
联系方式
地址:中国(上海)自由贸易试验区 外高桥美约路222号五楼501室
邮 编:200131
传 真:58661522
电 话:58661516
邮 箱:mdta@mdta.org.cn
下载专区
相关链接
©2018 上海浦东医疗器械贸易行业协会
沪ICP备19039930号-1 沪公网安备31019002000210号 互联网药品信息服务资格证书编号:(沪)-非经营性-2022-0001
技术支持:维程教育




 loading......
loading......